您好!欢迎访问洛阳富道生物科技有限公司官方网站!
抽象的
类风湿性关节炎 (RA) 是一种常见的自身免疫性疾病,其特征是慢性关节炎。其病理生理机制涉及免疫细胞间复杂的相互作用,导致关节损伤,主要累及滑膜。微小RNA (miR),即单链非编码RNA,在调控影响RA进展的通路中发挥着关键作用,尤其是在成纤维细胞样滑膜细胞和外周血单核细胞中。受miR影响的关键通路包括NF-κB、细胞凋亡、PI3K/AKT信号传导和细胞因子产生。失调的miR会影响细胞增殖、存活和炎症反应。本综述不仅探讨了miR在RA发病机制中的作用,还强调了其作为早期检测和严重程度预测生物标志物的潜力。此外,针对miR的治疗方法(包括模拟物和抑制剂)在动物模型中显示出良好的前景,其中关节内给药等方法因其疗效更佳、副作用更少而受到青睐。虽然早期研究强调了 RA 治疗的潜在途径,但将这些发现转化为安全有效的临床疗法仍然存在挑战。
关键词:
类风湿性关节炎;microRNA;滑膜细胞;治疗
1. 引言
类风湿关节炎 (RA) 是一种滑膜关节慢性自身免疫性疾病,可导致慢性炎症并最终导致关节进行性破坏 [ 1,2 ]。该病女性发病率高于男性,40-60 岁患者发病率最高 [ 3 ]。RA 患者通常表现为双侧多个关节疼痛和肿胀。疼痛伴有晨僵,可持续 1 小时以上 [ 4 ]。临床上通常根据欧洲抗风湿病联盟 (EULAR) 和美国风湿病学会 (ACR) 标准进行诊断 [ 5 ]。随着人口老龄化加快,RA 患病率不断上升,对全球医疗保健系统造成了沉重负担。
对该疾病分子通路的深入了解促进了新型治疗策略的开发,例如生物药物和小分子抑制剂[ 6 ]。尽管近期取得了这些成功,但仍有相当一部分患者出现令人衰弱的症状,并遭受进行性功能丧失和残疾的困扰。因此,需要进一步研究滑膜损伤背后的细胞和分子机制。
目前,我们对 RA 发病机制的理解涉及遗传、表观遗传和环境因素的共同作用,这些因素相互作用导致滑膜增生、炎症、进行性关节软骨退化和骨质侵蚀(图 1)[ 7 ]。虽然遗传因素(例如基因多态性)早已被确定为 RA 的危险因素和发病机制的要素 [ 8,9 ],但最近的研究一直在探索基因表达调控的表观遗传机制,例如微小 RNA (miR),作为疾病发展的潜在因素。
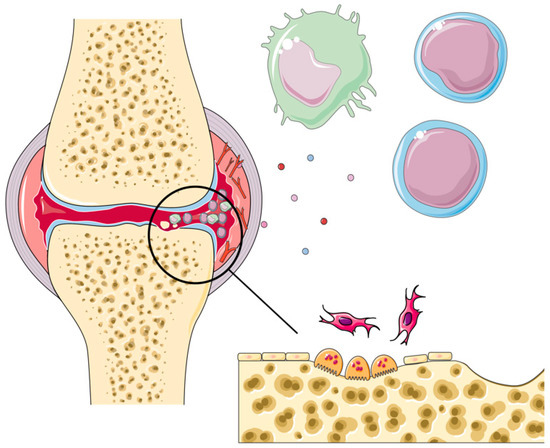
图 1. 类风湿关节炎发病机制的图示。类风湿关节炎的典型特征,例如持续性炎症、滑膜增生、关节组织退化和骨质侵蚀,是多种细胞类型相互作用的结果,例如抗原呈递细胞 (APC)、单核细胞(T 淋巴细胞和 B 淋巴细胞)、成纤维细胞样滑膜细胞 (FLS) 和软骨细胞。
证据表明,miR 能够影响参与多种分子过程的蛋白质表达,从而在很大程度上参与了疾病的发病机制 [ 10 , 11 ]。此外,多项研究表明,miR 水平可作为生物标志物,在临床症状出现之前检测疾病的存在,并预测疾病过程的严重程度和对治疗的反应 [ 12 ]。在本综述中,我们将重点关注那些探索 miR 影响疾病过程的潜在机制的研究,以及那些旨在识别特定 miR 作为疾病生物标志物的研究。我们通过 PubMed 和 Google Scholar 使用关键词“microRNA”和“类风湿性关节炎”搜索了 Medline 数据库。纳入了 2005 年 1 月至 2024 年 12 月发表的论文,以及纳入论文的相关参考文献。出版物的语言仅限于英语,但对研究类型没有限制。
来源:MDPI,原文地址:https://www.mdpi.com/1422-0067/26/20/9950